Jak często czujesz się pobudzony, łatwo się denerwujesz i denerwujesz między posiłkami? Jak często polegasz na kawie, aby utrzymać się przy życiu? Jak często masz trudności z koncentracją przed jedzeniem? Zapalenie jest istotną reakcją organizmu człowieka. Jest wyzwalany przez układ odpornościowy, aby chronić nas przed urazami, infekcjami i / lub chorobami. Co się jednak dzieje, gdy w organizmie człowieka występuje zbyt wiele stanów zapalnych? A co się stanie, jeśli w mózgu jest zbyt dużo stanu zapalnego?
Zapalenie nerwów może powodować różne problemy zdrowotne, takie jak niepokój, stres, depresja, mgła mózgowa, zmęczenie, a nawet letarg, wśród innych dobrze znanych objawów. Na szczęście istnieje jeden naturalny środek, który może pomóc znacznie zmniejszyć stan zapalny i poprawić funkcjonowanie mózgu. Według badań naukowych kurkumina może pomóc w zwalczaniu zapalenia nerwów. Celem poniższego artykułu jest omówienie przeciwzapalnego działania kurkuminy na mikroglej, zdrowie mózgu i dobre samopoczucie.
Spis treści
Przeciwzapalne działanie kurkuminy w komórkach mikrogleju
Abstrakcyjny
Kwas lipotejchojowy (LTA) indukuje cząsteczki neurozapalne, przyczyniając się do patogenezy chorób neurodegeneracyjnych. Dlatego hamowanie cząsteczek neurozapalnych można opracować jako metodę terapeutyczną. Chociaż wcześniejsze dane potwierdzają immunomodulujące działanie kurkuminy, podstawowe szlaki sygnałowe są w dużej mierze niezidentyfikowane. Tutaj zbadaliśmy właściwości przeciwzapalne kurkuminy w komórkach mikrogleju BV-2 stymulowanych LTA. Czynnik martwicy nowotworu cytokiny zapalnej-? Wydzielanie TNF-a, prostaglandyny E2 (PGE2) i tlenku azotu (NO) w komórkach mikrogleju indukowanych przez LTA było hamowane przez kurkuminę Kurkumina hamowała również indukowane przez LTA syntazy NO (iNOS) i cyklooksygenazę-2 (COX-2) Następnie nasze badania mechanistyczne wykazały, że kurkumina hamowała indukowaną przez LTA fosforylację kinazy białkowej aktywowanej mitogenem (MAPK), w tym ERK, p38, Akt i translokację NF-kB. Ponadto, indukowana przez kurkuminę hemeoksygenaza (HO)-1HO- 1 i ekspresja czynnika jądrowego 2 związanego z erytroidem 2 (Nrf-2) w komórkach mikrogleju. Hamowanie HO-1 odwróciło efekt hamowania HO-1 na mediatory zapalne uwalniane w komórkach mikrogleju stymulowanych LTA. Podsumowując, nasze wyniki sugerują że kurkumina może być potencjalnym środkiem terapeutycznym do leczenia zaburzeń neurodegeneracyjnych poprzez tłumienie odpowiedzi neurozapalnych. Słowa kluczowe: kurkumina, zapalenie nerwów, TLR2, HO-1, komórki mikrogleju
Wprowadzenie
Przewlekłe zapalenie nerwów odgrywa ważną rolę w różnych chorobach neurodegeneracyjnych, w tym AD, chorobie Parkinsona (PD), chorobie Huntingtona (HD), udarze, stwardnieniu zanikowym bocznym (ALS) i stwardnieniu rozsianym (MS) (Spangenberg i Green, 2017). Zapalenie nerwów jest przerywane przez aktywację mikrogleju, głównych komórek efektorowych i rezydentnych komórek odpornościowych OUN (Nakagawa i Chiba, 2015). Komórki mikrogleju mogą być aktywowane w odpowiedzi na śmierć neuronów lub uszkodzenie neuronów wywołane reakcjami neurozapalnymi lub toksynami zewnątrzkomórkowymi, takimi jak bakterie i patogeny (Larochelle i in., 2015). W zapaleniu nerwów aktywowany mikroglej uwalnia różne rodzaje cytokin, chemokin, reaktywnych form tlenu i reaktywnych form azotu w celu rozwoju i utrzymania odpowiedzi zapalnych (Moss i Bates, 2001). Nadmierna produkcja tych mediatorów stanu zapalnego może spowodować uszkodzenie neuronów i śmierć. Zgromadzone dowody sugerują, że kontrola aktywacji mikrogleju może złagodzić nasilenie choroby neurodegeneracyjnej (Perry i in., 2010). Dlatego opracowanie środków przeciwzapalnych, hamujących aktywację mikrogleju, może być korzystne w leczeniu chorób neurodegeneracyjnych.
Mikroglej eksprymuje receptory rozpoznawania wzorców (PRR), które mogą wiązać się z wzorcami molekularnymi związanymi z wzorcami (PAMP) i wzorcami molekularnymi związanymi z uszkodzeniami (DAMP), takimi jak odpowiednio lipopolisacharyd (LPS) i kwas lipotejchojowy (LTA) (Jack i in., 2005 ). TLR, główna klasa PRR, odgrywają kluczową rolę w obronie gospodarza poprzez indukowanie wrodzonych odpowiedzi immunologicznych. Coraz częściej badania wskazują, że agonista TLR2 LTA bierze udział w patogenezie chorób zakaźnych OUN i może indukować uszkodzenie neuronów (Neher i in., 2011). Hamowanie aktywacji TLR2 osłabia aktywację komórek mikrogleju i amyloid ? akumulacja w mózgu (McDonald i in., 2016; Hossain i in., 2017). W transdukcji sygnału przez TLR2 pośredniczą różne białka adaptorowe, w tym MyD88, które promuje przekazywanie sygnału w dół poprzez aktywację MAPK i NF-kB, prowadząc do ekspresji mediatorów stanu zapalnego (Larochelle i in., 2015).
Cząsteczki zapalne i utleniające są bardzo silnymi aktywatorami Keap-Nrf2 (czynnik 2 związany z NF-E2), który indukuje ekspresję enzymów detoksykacyjnych fazy II w celu dostosowania się do warunków stresu oksydacyjnego (Rojo i in., 2010). Zwykle Nrf2 działa w formie nieaktywnej. Po stymulacji Nrf2 oddziela się od Keap1 i przemieszcza się do jądra, gdzie wiąże się z elementem odpowiedzi antyoksydacyjnej (ARE), aby aktywować transkrypcję genów antyoksydacyjnych do ochrony cytoprotekcji (Ma, 2013; Cho i in., 2015). Jednym z genów regulowanych przez Nrf2 jest oksygenaza hemowa-1 (HO-1), która ma sekwencję ARE w swoim regionie promotorowym. Ostatnio doniesiono, że HO-1 jest dominującym czynnikiem w kontrolowaniu stresu oksydacyjnego i odpowiedzi zapalnych w chorobach neurodegeneracyjnych (Schipper i in., 2009). HO-1 jest pierwszym indukowalnym enzymem ograniczającym szybkość rozkładu hemu na produkty uboczne. HO-1 może zapewniać neuroprotekcję lub działanie neurotoksyczne ze względu na równowagę między korzystnym i toksycznym działaniem hemu i produktów hemu (Mancuso i in., 2010). Wykazano, że jeden produkt uboczny HO-1, bilirubina, chroni neurony przed stresem oksydacyjnym in vivo i in vitro. Bilirubina może zostać utleniona do biliwerdyny poprzez wychwytywanie rodników nadtlenowych (Chen, 2014). Sugerowano, że HO-1, biliwerdyna i CO mają właściwości przeciwzapalne (Jazwa i Cuadrado, 2010). Inne badanie sugeruje, że myszy pozbawione HO-1 były podatne na bodźce prozapalne i rozwinęły przewlekłe zapalenie z powodu obniżonego poziomu żelaza (Chora i in., 2007). Co więcej, ostatnie badanie sugeruje, że regulacja w górę szlaków Nrf2 i HO-1 znacząco hamuje reakcję zapalną w aktywowanym mikrogleju (Kim i in., 2016). Nrf2 hamował hiperaktywację mikrogleju poprzez tłumienie p38 MAPK i szlaku sygnałowego NF-kB (Kim BW i in., 2013). Wykazano, że powalenie Nrf2 u myszy jest nadwrażliwością na zapalenie nerwów, na co wskazuje wzrost markerów stanu zapalnego iNOS, IL-6 i TNF-a (Rojo i in., 2010). W konsekwencji Nrf2 i HO-1 zostały uznane za ważne cele terapeutyczne dla chorób neurodegeneracyjnych (Koh i in., 2011; Zhang i in., 2014).
Kurkumina, główny kurkuminoid wyizolowany z Curcuma longa L. (kurkuma), była stosowana od wieków w Azji Południowo-Wschodniej zarówno jako środek leczniczy, jak i pożywienie (Kunnumakkara i in., 2017). Kurkumina, demetoksykurkumina, bisdemetoksykurkumina, ar-turmeron, a-turmeron i a-turmeron to główne związki bioaktywne występujące w C. longa. We współczesnych badaniach farmakologicznych składniki C. longa, w szczególności kurkumina, wykazały obiecujące działania farmakologiczne ze względu na jej działanie przeciwzapalne, neuroprotekcyjne, chemoprewencyjne, immunomodulujące i potencjalnie chemoterapeutyczne (Garcia-Alloza i in., 2007; Zhou i in., 2017). Poprzednie badanie wykazało, że kurkumina hamowała reakcje zapalne indukowane przez LPS w makrofagach RAW264.7, co sugeruje potencjalną rolę kurkuminy w zakażeniach bakteriami anty-Gram-ujemnymi (Zhou i in., 2017), a zarówno badania in vivo, jak i in vitro wykazały że kurkumina wykazuje działanie przeciwzapalne (Garcia-Alloza i in., 2007; Prakobwong i in., 2011; Parada i in., 2015; Li i in., 2016). Ponadto doniesiono, że kurkumina promuje rozwój fenotypu mikrogleju M2 w sposób zależny od HO-1 i zmniejsza indukcję iNOS, chroniąc komórki mikrogleju przed stresem oksydacyjnym (Parada i in., 2015). W niniejszym badaniu zbadaliśmy, czy kurkumina może wpływać na aktywację mikrogleju indukowaną przez LTA. Ligand TLR2 LTA jest głównym składnikiem ściany komórkowej bakterii Gram-dodatnich. Pokazujemy, że kurkumina wykazuje działanie przeciwzapalne i przeciwutleniające w mikrogleju BV2 stymulowanym LTA poprzez aktywację mechanizmów cytoprotekcyjnych HO-1/Nrf2/ARE.
Materiały i Metody
Materiały
Kurkuminę i inne odczynniki zakupiono od firmy Sigma (C7727, >80%, St. Louis, MO, Stany Zjednoczone). Protoporfiryna IX (SnPP) i przeciwciała skierowane przeciwko HO-1 (sc-390991) – Nrf2 (sc-722), białko wiążące TATA (TBP; sc-74595), a-tubulina (sc-134237) i a-aktyna (sc-130065) – zakupiono od Santa Cruz Biotechnology, Inc., (Dallas, TX, Stany Zjednoczone). Przeciwciała skierowane przeciwko iNOS (13120) – fosforylowane (p)-MAPK (9910s), MAPK (9926), kinaza białkowa B (Akt; 4685), p-Akt (13038) i zestaw szlaku NF-kB (9936) – zostały zakupione od Cell Signaling Technology, Inc., (Danvers, MA, Stany Zjednoczone). LTA otrzymano z InvivoGen (tlrl-pslta, Tuluza, Francja). Dodatkowo, inhibitor JNK (inhibitor JNK II; 420119), inhibitor Akt (wortmannina; 12-338), inhibitor ERK (PD98059, 513000) i inhibitor p38 (SB230580, 559395) zakupiono od EMD Millipore (Billerica, MA, Stany Zjednoczone ). Pożywkę do hodowli komórkowej, DMEM i płodową surowicę bydlęcą (FBS) zakupiono od Gibco BRL (obecnie Invitrogen Corporation, Carlsbad, CA, Stany Zjednoczone).
Hodowlę komórkową
Mysie komórki mikrogleju BV-2 zakupiono od ATCC. Komórki hodowano w DMEM uzupełnionym 10% inaktywowanym termicznie FBS i 0.1% penicyliną-streptomycyną (BioSource International, Camarillo, CA, Stany Zjednoczone) w 37°C w wilgotnej atmosferze 5% CO2 i 95% powietrza.
Test żywotności komórek
Cytotoksyczność kurkuminy oceniano za pomocą testu kolorymetrycznego opartego na mikrohodowli [3-(4,5-dimetylotiazol-2-ilo)-2,5-difenylotetrazoliowy bromek] (MTT). Komórki inkubowano w 24-studzienkowych płytkach przy gęstości 5 x 105 komórek na studzienkę. Roztwór MTT (5 ml 5 mg/ml) dodano do każdej studzienki (końcowe stężenie 62.5 mg/ml). Po inkubacji przez 3 godziny w 37°C w 5% CO2, supernatant usunięto i kryształy formazanu wytworzone w żywych komórkach rozpuszczono w 150 ml sulfotlenku dimetylu (DMSO). Następnie odczytywano absorbancję każdej studzienki przy 570 nm przy użyciu czytnika mikropłytek (Wallac 1420; PerkinElmer, Inc., Boston, MA, Stany Zjednoczone).
Pomiar stężenia azotynów
Syntezę NO w hodowlach komórkowych mierzono metodą Griessa z mikropłytką. Aby zmierzyć azotyny, z kondycjonowanej pożywki pobrano 100-μl porcje i inkubowano z równą objętością odczynnika Griessa [1% sulfanilamidu/0.1% N-(1-naftylo)-etylenodiaminodichlorowodorku/2.5% H3PO4] w temperaturze pokojowej przez 10 minut. Stężenie azotynów określono przez pomiar absorbancji przy 540 nm za pomocą 96-dołkowego spektrofotometru do mikropłytek Vmax (Molecular Devices, Menlo Park, CA, Stany Zjednoczone). Jako wzorzec zastosowano azotyn sodu.
Pomiar TNF-? i Koncentracja PGE2
Komórki inkubowano najpierw z różnymi stężeniami kurkuminy przez 1 godzinę, a następnie z LTA przez 16 godzin. Po 24-godzinnej inkubacji TNF-? a poziomy PGE2 oznaczano ilościowo w pożywce hodowlanej stosując zestaw do testu immunoenzymatycznego (ELISA) (R&D Systems, Minneapolis, MN, Stany Zjednoczone) zgodnie z instrukcjami producenta.
Przygotowanie ekstraktu jądrowego
Komórki mikrogleju BV-2 przemyto trzykrotnie zimnym PBS i zebrano w 3000 ?l PBS stosując wirowanie przy 800 xg przez 5 min (4°C). Osady komórek zawieszono w buforze A [10 mM HEPES-KOH (pH 7.9); 1.5 mM MgCl2; 10 mM KCI; 0.5 mM ditiotreitol (DTT); 0.2 mM inhibitora proteazy (PI)] i inkubowano przez 5 minut na lodzie. Bufor B [10 mM HEPES-KOH (pH 7.9); 1.5 mM MgCl2; 420 mM NaCl; 0.2 mM EDTA; glicerol 25% v/v; 0.1 mM DTT; 0.2 mM PI] dodano do ekstraktu komórkowego i inkubowano na lodzie przez 5 minut przed odwirowaniem przy 11,000 1 xg przez 4 minutę w 10°C. Białka jądrowe ekstrahowano z dodatkiem kompletnego buforu do lizy B [7.9 mM HEPES-KOH (pH 1.5); 2 mM MgCl10; 0.5 mM KCI; 0.2 mM DTT; 25 mM PI; 420% (wag./obj.) gliceryna; 0.2 mM NaCl; 30 mM EDTA] przez 4 min w 11,000°C z okazjonalnym worteksowaniem. Po odwirowaniu przy 5 4 xg przez 70 minut w temperaturze XNUMX°C supernatanty zebrano i przechowywano w temperaturze -XNUMX°C.
Analiza Western Blot
Komórki BV-2 zebrano w lodowatym buforze do lizy (1% Triton X-100; 1% dezoksycholan; 0.1% dodecylosiarczan sodu). Następnie określono zawartość białka w lizatach komórkowych przy użyciu odczynnika Bradforda (zestaw Bio-Rad Protein Assay I5000001; Bio-Rad Laboratories, Inc., Hercules, CA, Stany Zjednoczone). Całkowite białka w każdej próbce (50 μg) rozdzielono za pomocą 7.5% SDS-PAGE i przeniesiono na membrany z difluorku poliwinylidenu. Po zablokowaniu niespecyficznych miejsc wiązania 5% odtłuszczonym mlekiem w temperaturze pokojowej przez 30 min, błony inkubowano z pierwszorzędowymi przeciwciałami skierowanymi przeciwko iNOS (1:500), p-Akt (1:1,000), p- MAPK (1:1,000), MAPK (1:1,000), p-p65, p65 (1:500), pI?B?, I?B? (1:1,000), HO-1 (1:1,000), Nrf2 (1:1,000), TBP (1:3,000), ? (1:1,000), HO-1 (1:1.0) i aktyna (1:3,000) przez 16 godzin w 4°C. Następnie inkubowano z drugorzędowymi przeciwciałami przeciwkróliczymi (sc-2768; 1:5,000) skoniugowanymi z peroksydazą chrzanową (sc-2371; 1:5,000) lub antymysimi (sc-1; 20:350) (Santa Cruz Biotechnology, Inc.) w temperaturze pokojowej przez XNUMX H. Tubulinę stosowano jako kontrolę ładowania dla każdej linii. Białka wizualizowano przy użyciu ulepszonego zestawu do wykrywania chemiluminescencji (GE Healthcare, Chicago, IL, Stany Zjednoczone). Po przemyciu PBS z Tween-XNUMX, prążki białkowe uwidoczniono stosując Gel Docs jako kontrolę obciążenia dla każdej ścieżki. Białka wizualizowano za pomocą analizatora Quant XNUMX (GE Healthcare).
RT-PCR w czasie rzeczywistym
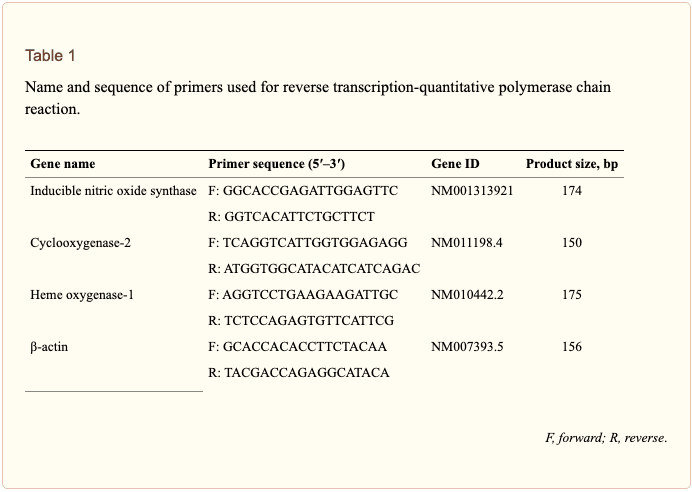
Całkowity RNA wyizolowano z komórek przy użyciu zestawu do izolacji RNA spin miniRNA (GE Healthcare, Uppsala, Szwecja) zgodnie z instrukcjami producenta. cDNA zsyntetyzowano z 1 ?g całkowitego RNA przy użyciu Maxime RT PreMix (Takara, Gyeonggi-do, Japonia) i zakotwiczonych starterów oligo-dT15. PCR w czasie rzeczywistym przeprowadzono przy użyciu instrumentu Chromo4TM (Bio-Rad) i SYBR Green Master Mix (Applied Biosystems, Foster City, CA, Stany Zjednoczone). Względne ilości docelowego mRNA określono stosując metodę progów porównawczych (Ct) przez normalizację wartości Ct docelowego mRNA do wartości dla a-aktyny (Ct). Pierwsze sekwencje stosowane w badaniu przedstawiono w Tabeli A1.
Analiza statystyczna
Dane wyrażono jako średnią (odchylenie standardowe, SD). Każdy eksperyment powtórzono co najmniej trzy razy. Analizę statystyczną przeprowadzono przy użyciu oprogramowania Statistical Package for GraphPad Prism (wersja 16.0) w celu określenia istotnych różnic. Do analiz wykorzystaliśmy test t-Studenta lub jednokierunkową analizę wariancji (ANOVA), a następnie testy post hoc Dunna. Wartości p < 0.05 uznano za istotne statystycznie.
Efekt
Kurkumina nie wpływała na żywotność komórek
Przeprowadzono eksperymenty żywotności komórek w celu ustalenia, czy stężenia kurkuminy zastosowane w tym badaniu wpłynęły na żywotność mikrogleju BV2. Figura a1 pokazuje, że kurkumina w stężeniu w zakresie 5-20 μM, razem z LTA lub bez niego, nie powodowała cytotoksyczności w mikrogleju BV5. Dlatego wykorzystaliśmy te stężenia kurkuminy do dalszych badań.
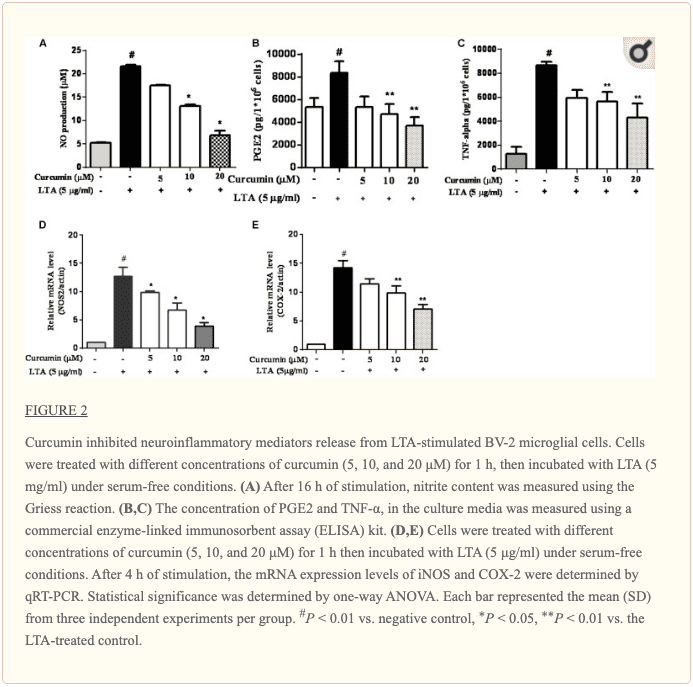
Kurkumina zapobiegała wytwarzaniu cząsteczek neurozapalnych w mikrogleju BV2 aktywowanym przez LTA
Aby zbadać wpływ kurkuminy na wydzielanie cytokin zapalnych, komórki BV2 traktowano LTA w obecności i nieobecności kurkuminy przez 24 godziny. Kurkumina nie została usunięta przed dodaniem LTA. Uwalnianie NO, PGE2 i TNF-? były znacząco i zależne od dawki zmniejszone przez kurkuminę (ryc. 2A – C). Ponadto LTA zwiększyło ekspresję mRNA iNOS i COX-2. Inkubacja z kurkuminą tłumiła ekspresję mRNA COX-2 i iNOS w komórkach mikrogleju BV2 stymulowanych przez LTA w sposób zależny od stężenia (ryc. 2D, E).
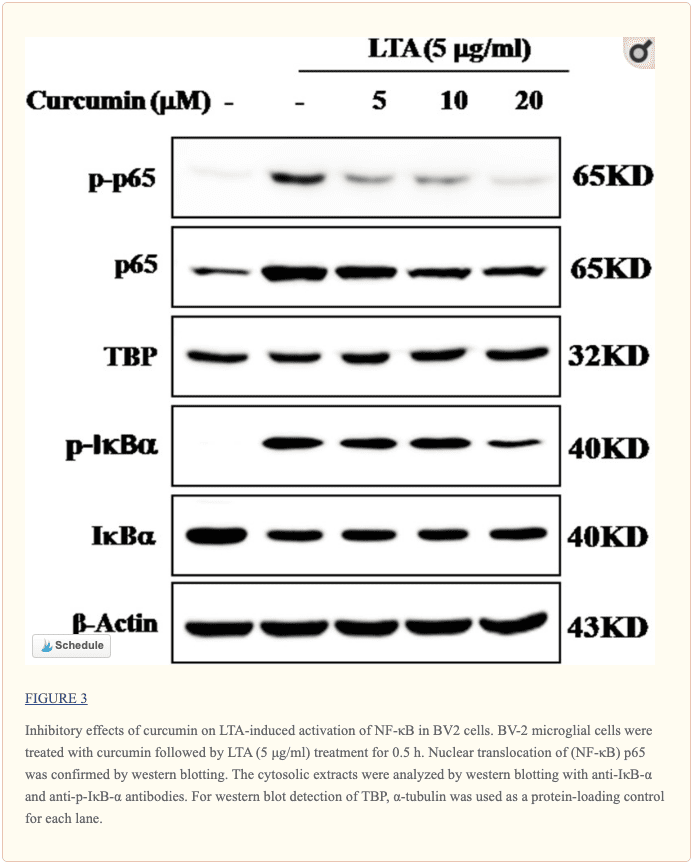
Stłumiona przez kurkuminę indukowana przez LTA aktywacja NF-kB w komórkach mikrogleju BV-2
Geny kodujące ekspresję białek zapalnych w odpowiedzi na aktywację mikrogleju znajdowały się pod kontrolą transkrypcji NF-kB. Dlatego zbadaliśmy wpływ kurkuminy na aktywację NF-kB w komórkach mikrogleju stymulowanych LTA. Wyniki pokazały, że LTA indukował charakterystyczny wzrost fosforylacji IkBp. Po wstępnym potraktowaniu kurkuminą poziomy pIkB? były znacznie zmniejszone w sposób zależny od stężenia (Rysunek ?3 i Rysunek dodatkowy S1). Konsekwentnie, translokacja jądrowa podjednostki NF-kB p65 indukowana przez LTA była również osłabiona przez wstępne potraktowanie kurkuminą. Podsumowując, kurkumina prawdopodobnie osłabia ekspresję cząsteczek neurozapalnych poprzez hamowanie translokacji jądrowej i aktywacji NF-kB. Kwantyfikacja wraz z analizą statystyczną została dostarczona jako dane pomocnicze.
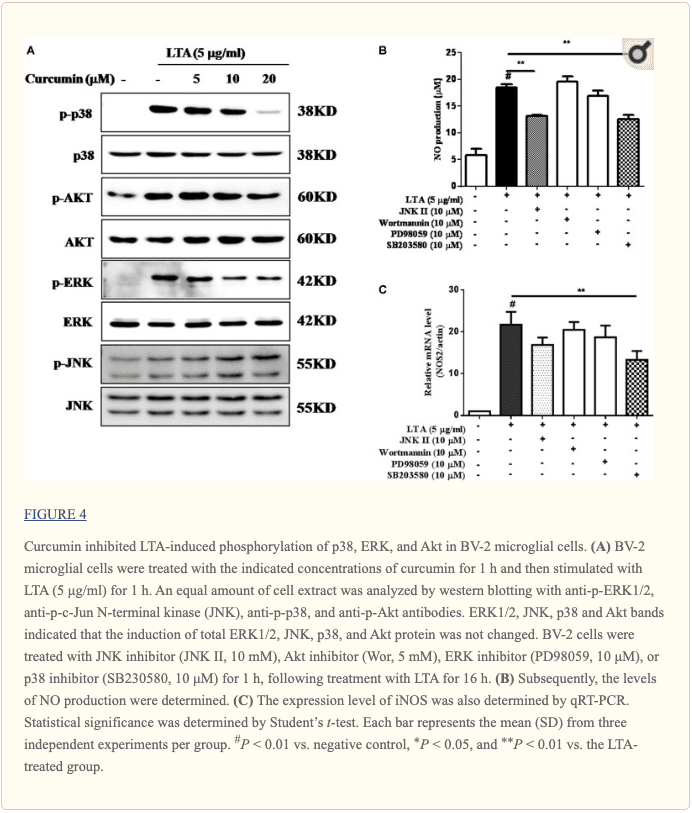
Kurkumina Indukowana przez LTA aktywacja p38 i ERK MAPK w komórkach mikrogleju BV-2
Oprócz NF-kB, MAPK są również modulatorami upstream cząsteczek neurozapalnych w komórkach mikrogleju. Wcześniejsze badania wykazały, że kurkumina antagonizowała indukowaną przez LPS fosforylację MAPK w mikrofagach (Yang i in., 2008; Kunnumakkara i in., 2017). Aby zbadać, czy kurkumina hamuje zapalenie nerwów poprzez regulację MAPK, zbadaliśmy jej wpływ na indukowaną przez LTA fosforylację MAPK. Komórki mikrogleju BV-2 traktowano wstępnie różnymi stężeniami kurkuminy przez 3 godziny, a następnie stymulowano LTA przez 1 godzinę. Jak pokazano na rysunku A4A i rysunku dodatkowym S2, kurkumina hamowała indukowaną przez LTA fosforylację ERK, p38 i Akt. Jednak do 20 μM kurkuminy nie wpływało na fosforylację JNK indukowaną przez LTA. Doniesiono, że szlak MAPK pośredniczy w wytwarzaniu cytokin, chemokin i innych cząsteczek neurozapalnych. Dlatego następnie zbadaliśmy rolę ERK, p38, JNK i Akt w wytwarzaniu cząsteczek neurozapalnych komórek BV2 przy użyciu inhibitorów ERK, p38, JNK i Akt. Jednak tylko inhibitor p38 SB203580 znacząco zmniejszył indukowane przez LTA uwalnianie poziomów ekspresji NO i mRNA iNOS (ryc. 4B, C). Chociaż kurkumina nie hamowała fosforylacji JNK, inhibitor JNK II znacząco hamował uwalnianie NO indukowane przez LTA (Figura A4B). Wyniki sugerują, że szlaki sygnalizacyjne MAPK są zaangażowane w działanie przeciwzapalne kurkuminy w mikrogleju stymulowanym LTA. Kwantyfikacja wraz z analizą statystyczną jest dostarczona jako dane pomocnicze.
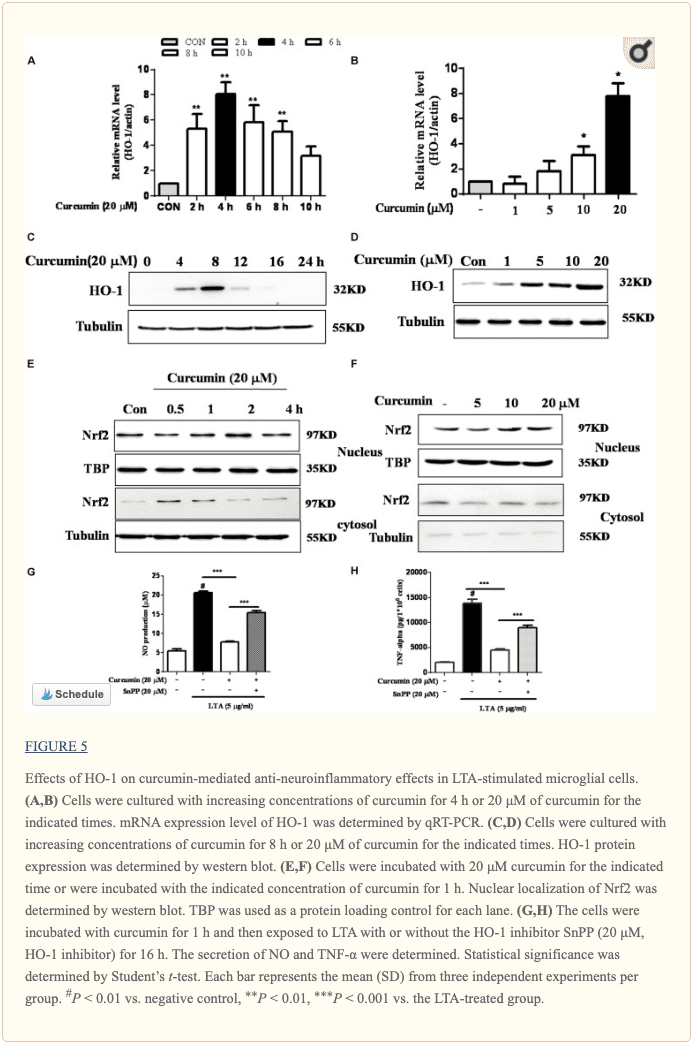
Hamowanie sygnalizacji HO-1 znosi hamujący wpływ kurkuminy na odpowiedzi neurozapalne
HO-1 działa jako modulator przeciwzapalny i przeciwutleniający w mikrogleju (Schipper i in., 2009). Analizy Western blot i RT-PCR wykazały, że kurkumina zwiększała ekspresję HO-1 na poziomach białka i mRNA, jak pokazano na rysunkach 5A – D i rysunku uzupełniającym S3. Ekspresja mRNA i białka HO-1 była maksymalnie zwiększona w komórkach mikrogleju BV-2 traktowanych 20 µM kurkuminą odpowiednio przez 4 godziny i 8 godzin. Ponadto kurkumina zwiększyła translokację jądrową Nrf2 w ciągu 1 godziny i przedłużyła stan translokacji jądrowej do 2 godzin (ryc. 5E, F i rysunek dodatkowy S3). Następnie zbadaliśmy, czy indukowana kurkuminą HO-1 pośredniczy w odpowiedzi przeciwzapalnej w komórkach mikrogleju BV-2 stymulowanych LTA. Traktowaliśmy komórki inhibitorem HO-1 SnPP. Następnie oceniliśmy wpływ kurkuminy na indukowane przez LTA NO i TNF-? uwolnienie. Traktowanie SnPP znacząco hamowało hamowanie, w którym pośredniczy kurkumina uwalniania NO i TNF-α (ryc. 5G, H). Podsumowując, wyniki te ujawniają, że zależna od kurkuminy aktywacja sygnału HO-1 i Nrf-2 odgrywa kluczową rolę w zmniejszaniu odpowiedzi neurozapalnych. Kwantyfikacja wraz z analizą statystyczną jest dostarczona jako dane pomocnicze.
Dyskusja
Doniesiono, że mikroglej, główne makrofagi rezydujące w OUN, są głównymi komórkami efektorowymi w pośredniczeniu w zapaleniu nerwów i selektywnej śmierci neuronów (Perry i in., 2010). Komórki mikrogleju zwiększają produkcję cząsteczek neurozapalnych po ekspozycji na aktywatory, takie jak LPS i LTA, poprzez ich receptory powierzchniowe, odpowiednio, TLR4 i TLR2 (Perry i Holmes, 2014; Hossain i in., 2017). Zwiększona ekspresja i aktywacja TLR2 jest związana z postępem chorób neurodegeneracyjnych, takich jak PD i demencja (Dzamko i in., 2017). Na przykład aktywacja TLR2 może regulować w górę a-synukleinę w mózgach PD i odgrywać ważną rolę w patogenezie mózgów PD (Roodveldt i in., 2013). Ponadto Kim C. i in. (2013) wykazali również, że neurodegeneracja była osłabiana przez nokaut lub nokaut TLR2 w modelach PD u gryzoni. Zatem kontrolowanie aktywacji mikrogleju za pośrednictwem TLR2 i neurotoksyczności zostało zasugerowane jako ważne podejście terapeutyczne do leczenia chorób neurodegeneracyjnych. Potencjalnym czynnikiem w tym procesie może być kurkumina, której działanie neuroochronne i przeciwzapalne wykazano w różnych modelach eksperymentalnych (Parada i in., 2015; Li i in., 2016). Kurkumina jest wysoce lipofilowym naturalnym związkiem. Poprzednie badanie dobrze wykazało, że kurkumina jest w stanie przekroczyć barierę krew-mózg i że koncentruje się głównie w hipokampie w mózgu (Tsai i in., 2011). Niektóre badania wykazały, że kurkumina hamuje uszkodzenia neuronów wywołane gp1 przez HIV-120 i zapewnia działanie przeciwzapalne w mikrogleju indukowanym przez LPS (Gong i in., 2012). Ten ochronny efekt kurkuminy wydaje się być zależny od jej działania przeciwzapalnego. Kurkumina może chronić neurony przed neurotoksycznością za pośrednictwem mikrogleju, stając się jednocześnie nieskuteczna w warunkach zubożenia mikrogleju (Park i in., 2001; Yang i in., 2008; Parada i in., 2015). Podobne badania na komórkach obwodowych wykazały również przeciwzapalne działanie kurkuminy. Badania wykorzystujące mysie makrofagi RAW 264.7 wykazały, że kurkumina hamuje PGE2, NO i TNF-? uwalnianie po stymulacji LPS (Pae i in., 2008). Jednak wpływ kurkuminy na zapalenie nerwów wywołane przez TLR2 w komórkach mikrogleju nie jest w pełni zrozumiały.
Regulacja szlaków sygnałowych w aktywowanym mikrogleju jest ważna dla utrzymania homeostazy OUN, ponieważ rozregulowane odpowiedzi neurozapalne mogą skutkować śmiercią sąsiednich neuronów poprzez uwolnienie cząsteczek zapalnych, takich jak cytokiny, chemokiny, NO i RFT (Perry i Holmes, 2014; Spangenberg i Green, 2017). Na przykład nadmierna synteza NO pod wpływem endotoksyn powoduje powstawanie reaktywnych form azotu i śmierć komórek nerwowych (Perry i in., 2010). Wykazano również, że PGE2 przyczynia się do śmierci neuronów poprzez aktywację szlaku MAPK/ERK w mikrogleju (Xia i in., 2015). W tym badaniu wykazaliśmy, że kurkumina hamuje wydzielanie mediatorów zapalnych TNF-a, NO i PGE2 oraz ekspresję iNOS i COX-2 w mikrogleju BV2 stymulowanym LTA. Ponadto wykazaliśmy, że kurkumina osłabia te efekty LTA bez zmiany przeżycia komórek, co sugeruje, że kurkumina jest bezpieczna i może być uważana za potencjalny środek terapeutyczny w stanach zapalnych układu nerwowego.
NF-kB jest głównym czynnikiem transkrypcyjnym, który odgrywa kluczową rolę w regulacji homeostazy redoks. NF-kB jest uważany za główny regulator reakcji zapalnych mikrogleju na uszkodzenie neuronów (Acharyya i in., 2007). Ostatnie badania wykazały, że aktywacja NF-kB kontroluje ekspresję cząsteczek zapalnych, takich jak NO, PGE2 i TNF-a, oraz wytwarzanie IL-1b (Acharyya i in., 2007). Zatem modulacja aktywacji NF-kB jest uważana za krytyczny sposób kontrolowania aktywacji mikrogleju. W aktywacji szlaku sygnałowego NF-kB pośredniczy białko IkB. Fosforylacja IkB powoduje dysocjację NF-kB, co prowadzi do indukcji mediatorów stanu zapalnego. W tym badaniu wykazano, że kurkumina wytwarza podwójne hamowanie fosforylacji i degradacji IkB, jak również translokację jądrową p65, co sugeruje, że ten czynnik może stabilizować NF-kB w cytoplazmie mikrogleju po stymulacji LTA w BV -2 komórki mikrogleju.
W komórkach ssaków szlaki sygnalizacyjne MAPK, w tym ERK, JNK i p38, przyczyniają się do produkcji szerokiej gamy mediatorów neurozapalnych (Chantong i in., 2014). W tym badaniu wstępne leczenie kurkuminą zmniejszyło fosforylację p38 i ERK. Ponadto inhibitor p38 SB203580 znacznie zmniejszał wydzielanie NO i ekspresję mRNA kluczowego genu prozapalnego, iNOS. Wyniki te sugerują, że kurkumina inicjowała działanie przeciwzapalne w komórkach mikrogleju BV-2 stymulowanych LTA, częściowo poprzez hamowanie aktywacji p38 MAPK. Szlak sygnałowy zależny od PI3K/Akt promuje reakcje zapalne w mikrogleju. Wykazano udział szlaku Akt w ekspresji mediatorów stanu zapalnego w mikrogleju poprzez aktywację NF-kB w mikrogleju (Lo i in., 2015). Kurkumina hamowała fosforylację Akt, dalszy cel PI3K. Jednak wortmannina będąca inhibitorem PI3K nie wykazywała żadnego działania hamującego na wydzielanie NO lub ekspresję mRNA iNOS. Podsumowując, dane te sugerują, że przeciwneurozapalne działanie kurkuminy występuje głównie poprzez hamowanie sygnalizacji NF-kB i MAPK.
Zidentyfikowaliśmy również szlak wewnątrzkomórkowy, który negatywnie reguluje ekspresję cząsteczek zapalnych w komórkach mikrogleju. Nrf2 jest wrażliwym na redoks czynnikiem transkrypcyjnym, który reguluje odpowiedzi zapalne mikrogleju na infekcje mózgu. Wpływ Nrf2 został opisany w różnych modelach in vivo, w których knockdown Nrf2 u myszy zwiększał podatność na astmę lub rozedmę płuc (Ma, 2013). Ponadto agonista TLR2 / TLR4 promował odpowiedzi zapalne u myszy Nrf2 KO w porównaniu z myszami WT (Kong i in., 2011). W obecnym badaniu wykazaliśmy, że kurkumina zwiększa ekspresję Nrf2 i jego dalszego białka HO-1. HO-1 jest kluczową cząsteczką sygnalizacyjną zaangażowaną w regulację odpowiedzi zapalnych i oksydacyjnych. Gen HO-1 ma w swoim regionie promotorowym sekwencję ARE, która jest miejscem wiązania czynnika transkrypcyjnego Nrf2. Kilka badań sugerowało, że NF-kB przerywa szlak sygnałowy Nrf-2-ARE, ponieważ wiele związków, które indukowały sygnalizację HO-1 i Nrf2, przypadkowo tłumiło aktywację NF-kB (Li i in., 2016). Ekspresja HO-1 była niezbędna dla efektu cytoprotekcyjnego specyficznego dla mikrogleju (Parada i in., 2015). Kilka badań wykazało również odwrotną korelację między wydzielaniem HO-1 a mediatorem zapalnym (Chora i in., 2007; Parada i in., 2015). W zgodzie zaobserwowaliśmy, że sama kurkumina indukowała ekspresję HO-1 w komórkach mikrogleju. Co więcej, inhibitor HO-1 zniósł działanie przeciwzapalne kurkuminy w komórkach mikrogleju BV-2.
Wnioski
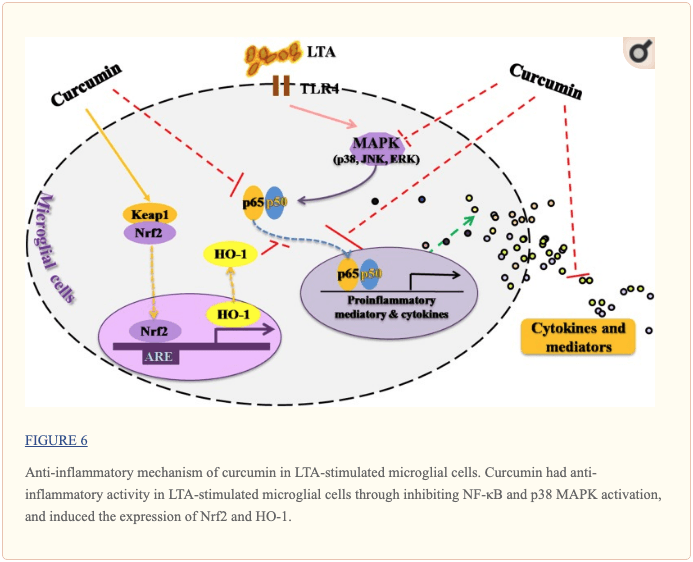
Badanie to wykazało, że kurkumina ma działanie przeciwzapalne w stymulowanych LTA komórkach mikrogleju, które mogą poprzez hamowanie aktywacji NF-kB i p38 MAPK i mogą indukować ekspresję Nrf2 i HO-1 (ryc. ?6). Ponadto kurkumina nie ma działania cytotoksycznego w komórkach mikrogleju BV-2 w dawce przeciwzapalnej. Kurkumina może mieć potencjał terapeutyczny w przypadku niektórych zaburzeń związanych z zapaleniem nerwów wywołanych przez bakterie Gram-dodatnie.

Kurkumina lub kurkuma jest silnym środkiem przeciwzapalnym, który, jak wykazano, ma wiele korzyści zdrowotnych. Uważana za przeciwutleniacz o właściwościach przeciwnowotworowych, przeciwdepresyjnych i przeciwstarzeniowych, kurkumina może znacznie więcej niż leczyć rany i poprawiać pamięć. Według badań naukowych kurkumina lub kurkuma mogą pomóc zmniejszyć zapalenie nerwów lub zapalenie mózgu. Ten silny środek przeciwzapalny może blokować produkcję cytokin prozapalnych i promować ogólne samopoczucie. – Dr Alex Jimenez DC, CCST Insight
Formularz oceny neuroprzekaźnika
Poniższy formularz oceny neuroprzekaźników można wypełnić i przedstawić dr Alexowi Jimenezowi. Objawy wymienione w tym formularzu nie są przeznaczone do diagnozowania jakiegokolwiek rodzaju choroby, stanu lub innego rodzaju problemu zdrowotnego.
Na cześć proklamacji gubernatora Abbotta, październik jest Miesiącem Zdrowia Chiropraktyki. Dowiedz się więcej o propozycja.
Jak często czujesz się pobudzony, łatwo się denerwujesz i denerwujesz między posiłkami? Jak często polegasz na kawie, aby utrzymać się przy życiu? Jak często masz trudności z koncentracją przed jedzeniem? Zapalenie jest ważną reakcją organizmu człowieka. Jest aktywowany przez układ odpornościowy, aby chronić nas przed urazami, infekcjami i / lub chorobami. Co się jednak dzieje, gdy w organizmie człowieka występuje zbyt wiele stanów zapalnych? A co się stanie, jeśli w mózgu jest zbyt dużo stanu zapalnego?
Zapalenie mózgu może powodować różne problemy zdrowotne, takie jak niepokój, stres, depresja, mgła mózgowa, zmęczenie, a nawet letarg, wśród innych typowych objawów. Na szczęście istnieje jeden naturalny środek, który może znacznie zmniejszyć zapalenie nerwów i poprawić funkcjonowanie mózgu. Według badań naukowych kurkumina może zwalczać zapalenie mózgu. Celem powyższego artykułu było omówienie przeciwzapalnego działania kurkuminy na mikroglej i dobre samopoczucie mózgu
Poniższy artykuł został przywołany z Narodowe Centrum Informacji Biotechnologicznej (NCBI). Zakres naszych informacji jest ograniczony do zagadnień dotyczących chiropraktyki, układu mięśniowo-szkieletowego i układu nerwowego lub artykułów, tematów i dyskusji dotyczących medycyny funkcjonalnej. Stosujemy funkcjonalne protokoły zdrowotne w leczeniu urazów lub zaburzeń układu mięśniowo-szkieletowego. Aby dokładniej omówić powyższy temat, prosimy zapytać dr Alexa Jimeneza lub skontaktować się z nami pod adresem 915-850-0900 .
Kurator: dr Alex Jimenez
1. Acharyya S., Villalta SA, Bakkar N., Bupha-Intr T., Janssen PM, Carathers M. i in. (2007). Wzajemne oddziaływanie sygnalizacji IKK/NF-kappaB w makrofagach i włóknach mięśniowych sprzyja degeneracji mięśni w dystrofii mięśniowej Duchenne'a. J. Clin. Inwestować. 117 889–901. 10.1172/JCI30556 [PMC bezpłatny artykuł] [PubMed] [CrossRef] [Google Scholar]
2. Chantong B., Kratschmar DV, Lister A., Odermatt A. (2014). Dibutylocyna promuje stres oksydacyjny i zwiększa mediatory stanu zapalnego w komórkach mikrogleju BV-2. Toksykol. Łotysz. 230 177–187. 10.1016/j.toxlet.2014.03.001 [PubMed] [CrossRef] [Google Scholar]
3. Chen J. (2014). Oksygenaza hemowa w neuroprotekcji: od mechanizmów do implikacji terapeutycznych. Wielebny Neurosci. 25 269–280. 10.1515/revneuro-2013-0046 [PubMed] [CrossRef] [Google Scholar]
4. Cho H., Hartsock MJ, Xu Z., He M., Duh EJ (2015). Fumaran monometylu promuje zależną od Nrf2 neuroprotekcję w reperfuzji niedokrwiennej siatkówki. J. Neuroinflamm. 12:239. 10.1186/s12974-015-0452-z [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
5. Chora AA, Fontoura P., Cunha A., Pais TF, Cardoso S., Ho PP i in. (2007). Oksygenaza hemowa-1 i tlenek węgla hamują autoimmunologiczne zapalenie nerwów. J. Clin. Inwestować. 117 438–447. 10.1172/JCI28844 [PMC bezpłatny artykuł] [PubMed] [CrossRef] [Google Scholar]
6. Dzamko N., Gysbers A., Perera G., Bahar A., Shankar A., Gao J. i in. (2017). Receptor Toll-podobny 2 jest zwiększony w neuronach w mózgu z chorobą Parkinsona i może przyczyniać się do patologii alfa-synukleiny. Acta Neuropathol. 133 303–319. 10.1007/s00401-016-1648-8 [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
7. Garcia-Alloza M., Borrelli LA, Rozkalne A., Hyman BT, Bacskai BJ (2007). Kurkumina oznacza patologię amyloidu in vivo, niszczy istniejące blaszki miażdżycowe i częściowo przywraca zniekształcone neuryty w modelu myszy z chorobą Alzheimera. J. Neurochem. 102 1095–1104. 10.1111/j.1471-4159.2007.04613.x [PubMed] [CrossRef] [Google Scholar]
8. Gong Z., Yang L., Tang H., Pan R., Xie S., Guo L. i in. (2012). Ochronne działanie kurkuminy przeciwko ludzkiemu wirusowi niedoboru odporności 1 wywołanemu pętlą uszkodzenia neuronów gp120 V3 u szczurów. Regeneracja neuronów. Rez. 7 171–175. 10.3969/j.issn.1673-5374.2012.03.002 [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
9. Hossain MJ, Tanasescu R., Gran B. (2017). Wrodzona regulacja immunologiczna autoimmunizacji w stwardnieniu rozsianym: ognisko na roli Toll-podobnego receptora 2. J. Neuroimmunol. 304 11–20. 10.1016/j.jneuroim.2016.12.004 [PubMed] [CrossRef] [Google Scholar]
10. Jack CS, Arbor N., Manusow J., Montgrain V., Blain M., McCrea E. i in. (2005). Sygnalizacja TLR dostosowuje wrodzone odpowiedzi immunologiczne w ludzkim mikrogleju i astrocytach. J. Immunol. 175 4320–4330. 10.4049/jimmunol.175.7.4320 [PubMed] [CrossRef] [Google Scholar]
11. Jazwa A., Cuadrado A. (2010). Ukierunkowanie na oksygenazę hemową-1 do neuroprotekcji i zapalenia nerwów w chorobach neurodegeneracyjnych. bież. Cele narkotykowe 11 1517–1531. 10.2174/1389450111009011517 [PubMed] [CrossRef] [Google Scholar]
12. Kim BW, Koppula S., Hong SS, Jeon SB, Kwon JH, Hwang BY i in. (2013). Regulacja aktywności mikrogleju przez glaukokaliksynę-A: osłabienie zapalenia nerwów stymulowanego lipopolisacharydem przez szlaki sygnałowe NF-kappaB i p38 MAPK. PLoS One 8:e55792. 10.1371/journal.pone.0055792 [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
13. Kim C., Ho DH, Suk JE, You S., Michael S., Kang J. i in. (2013). Uwalniana przez neurony oligomeryczna alfa-synukleina jest endogennym agonistą TLR2 do parakrynnej aktywacji mikrogleju. Nat. Komuna. 4:1562. 10.1038/ncomms2534 [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
14. Kim HJ, Kang CH, Jayasooriya RG, Dilshara MG, Lee S., Choi YH i in. (2016). Hydrangenol hamuje indukowaną lipopolisacharydem produkcję tlenku azotu w komórkach mikrogleju BV2 poprzez hamowanie szlaku NF-kappaB i aktywację szlaku HO-2, w którym pośredniczy Nrf1. Int. Immunofarmakol. 35 61–69. 10.1016/j.intimp.2016.03.022 [PubMed] [CrossRef] [Google Scholar]
15. Koh K., Kim J., Jang YJ, Yoon K., Cha Y., Lee HJ i in. (2011). Czynnik transkrypcyjny Nrf2 hamuje indukowaną przez LPS hiperaktywację komórek mikrogleju BV-2. J. Neuroimmunol. 233 160–167. 10.1016/j.jneuroim.2011.01.004 [PubMed] [CrossRef] [Google Scholar]
16. Kong X., Thimmulappa R., Craciun F., Harvey C., Singh A., Kombairaju P. i in. (2011). Wzmocnienie szlaku Nrf2 poprzez przerwanie Keap1 w leukocytach szpikowych chroni przed posocznicą. Jestem. J. Respir. Krytyk. Pielęgnacja med. 184 928–938. 10.1164/rccm.201102-0271OC [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
17. Kunnumakkara AB, Bordoloi D., Padmavathi G., Monisha J., Roy NK, Prasad S. i in. (2017). Kurkumina, złoty nutraceutyk: multitargeting dla wielu chorób przewlekłych. br. J. Pharmacol. 174 1325–1348. 10.1111/bph.13621 [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
18. Larochelle A., Bellaviance MA, Rivest S. (2015). Rola białka adaptorowego MyD88 w warunkowaniu wstępnym za pośrednictwem TLR i neuroprotekcji po ostrej ekscytotoksyczności. Zachowanie mózgu. odporność 46 221–231. 10.1016/j.bbi.2015.02.019 [PubMed] [CrossRef] [Google Scholar]
19. Li W., Suwanwela NC, Patumraj S. (2016). Kurkumina poprzez regulację w dół NF-kB i podniesienie Nrf2 zmniejsza obrzęk mózgu i dysfunkcję neurologiczną po I/R mózgu. mikronaczyni. Rez. 106 117–127. 10.1016/j.mvr.2015.12.008 [PubMed] [CrossRef] [Google Scholar]
20. Lo JY, Kamarudin MN, Hamdi OA, Awang K., Kadir HA (2015). Kurkumenol wyizolowany z Curcuma zedoaria hamuje aktywację NF-kappaB za pośrednictwem Akt i szlak sygnałowy p38 MAPK w komórkach mikrogleju BV-2 stymulowanych LPS. Funkcja żywności. 6 3550–3559. 10.1039/c5fo00607d [PubMed] [CrossRef] [Google Scholar]
21. Ma Q. (2013). Rola nrf2 w stresie oksydacyjnym i toksyczności. rok Wielebny Pharmacol. 53 401–426. 10.1146/annurev-pharmtox-011112-140320 [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
22. Mancuso C., Navarra P., Preziosi P. (2010). Role tlenku azotu, tlenku węgla i siarkowodoru w regulacji osi podwzgórze-przysadka-nadnercza. J. Neurochem. 113 563–575. 10.1111/j.1471-4159.2010.06606.x [PubMed] [CrossRef] [Google Scholar]
23. McDonald CL, Hennessy E., Rubio-Araiz A., Keogh B., McCormack W., McGuirk P. i in. (2016). Hamowanie aktywacji TLR2 osłabia akumulację amyloidu i aktywację gleju w mysim modelu choroby Alzheimera. Zachowanie mózgu. odporność 58 191–200. 10.1016/j.bbi.2016.07.143 [PubMed] [CrossRef] [Google Scholar]
24. Moss DW, Bates TE (2001). Aktywacja mysich linii komórkowych mikrogleju przez lipopolisacharyd i interferon gamma powoduje zależne od NO spadki funkcji mitochondriów i komórek. Eur. J. Neurosci. 13 529–538. 10.1046/j.1460-9568.2001.01418.x [PubMed] [CrossRef] [Google Scholar]
25. Nakagawa Y., Chiba K. (2015). Różnorodność i plastyczność komórek mikrogleju w zaburzeniach psychicznych i neurologicznych. Farmakol. Ter. 154 21-35. 10.1016/j.pharmthera.2015.06.010 [PubMed] [CrossRef] [Google Scholar]
26. Neher JJ, Neniskyte U., Zhao JW, Bal-Price A., Tolkovsky AM, Brown GC (2011). Zahamowanie fagocytozy mikrogleju jest wystarczające, aby zapobiec zapalnej śmierci neuronów. J. Immunol. 186 4973–4983. 10.4049/jimmunol.1003600 [PubMed] [CrossRef] [Google Scholar]
27. Pae HO, Jeong SO, Kim HS, Kim SH, Song YS, Kim SK i in. (2008). Dimetoksykurkumina, syntetyczny analog kurkuminy o wyższej stabilności metabolicznej, hamuje wytwarzanie NO, indukowalną ekspresję syntazy NO i aktywację NF-kB w makrofagach RAW264.7 aktywowanych LPS. Mol. Nutr. Żywność Rez. 52 1082–1091. 10.1002/mnfr.200700333 [PubMed] [CrossRef] [Google Scholar]
28. Parada E., Buendia I., Navarro E., Avendano C., Egea J., Lopez MG (2015). Indukcja mikrogleju HO-1 przez kurkuminę zapewnia działanie przeciwutleniające, przeciwzapalne i glioprotekcyjne. Mol. Nutr. Żywność Rez. 59 1690-1700. 10.1002/mnfr.201500279 [PubMed] [CrossRef] [Google Scholar]
29. Park LC, Zhang H., Gibson GE (2001). Wspólna hodowla z astrocytami lub mikroglejem chroni metabolicznie upośledzone neurony. Mech. Starzejący się Dev. 123 21–27. 10.1016/S0047-6374(01)00336-0 [PubMed] [CrossRef] [Google Scholar]
30. Perry VH, Holmes C. (2014). Priming mikrogleju w chorobie neurodegeneracyjnej. Nat. ks. Neurol. 10 217–224. 10.1038/nrneurol.2014.38 [PubMed] [CrossRef] [Google Scholar]
31. Perry VH, Nicoll JA, Holmes C. (2010). Mikroglej w chorobie neurodegeneracyjnej. Nat. ks. Neurol. 6 193–201. 10.1038/nrneurol.2010.17 [PubMed] [CrossRef] [Google Scholar]
32. Prakobwong S., Khoontawad J., Yongvanit P., Pairojkul C., Hiraku Y., Sithithaworn P. i in. (2011). Kurkumina zmniejsza cholangiocarcinogenezę u chomików poprzez tłumienie zdarzeń molekularnych, w których pośredniczy zapalenie, związanych z wieloetapową karcynogenezą. Int. J. Rak 129 88–100. 10.1002/ijc.25656 [PubMed] [CrossRef] [Google Scholar]
33. Rojo AI, Innamorato NG, Martin-Moreno AM, De Ceballos ML, Yamamoto M., Cuadrado A. (2010). Nrf2 reguluje dynamikę mikrogleju i zapalenie nerwów w eksperymentalnej chorobie Parkinsona. Glia 58 588–598. 10.1002/glia.20947 [PubMed] [CrossRef] [Google Scholar]
34. Roodveldt C., Labrador-Garrido A., Gonzalez-Rey E., Lachaud CC, Guilliams T., Fernandez-Montesinos R., et al. (2013). Wstępne kondycjonowanie mikrogleju przez alfa-synukleinę silnie wpływa na odpowiedź indukowaną przez stymulację receptora toll-like (TLR). PLoS One 8:e79160. 10.1371/journal.pone.0079160 [PMC bezpłatny artykuł] [PubMed] [CrossRef] [Google Scholar]
35. Schipper HM, Song W., Zukor H., Hascalovici JR, Zeligman D. (2009). Oksygenaza hemowa-1 i neurodegeneracja: poszerzanie granic zaangażowania. J. Neurochem. 110 469–485. 10.1111/j.1471-4159.2009.06160.x [PubMed] [CrossRef] [Google Scholar]
36. Spangenberg EE, Green KN (2017). Zapalenie w chorobie Alzheimera: wnioski wyciągnięte z modeli zubożenia mikrogleju. Zachowanie mózgu. odporność 61 1–11. 10.1016/j.bbi.2016.07.003 [darmowy artykuł na PMC] [PubMed] [CrossRef] [Google Scholar]
37. Tsai YM, Chien CF, Lin LC, Tsai TH (2011). Kurkumina i jej nanopreparat: kinetyka dystrybucji w tkankach i penetracja bariery krew-mózg. Int. J. Pharm. 416 331–338. 10.1016/j.ijpharm.2011.06.030 [PubMed] [CrossRef] [Google Scholar]
38. Xia Q., Hu Q., Wang H., Yang H., Gao F., Ren H. i in. (2015). Indukcja syntezy COX-2-PGE2 przez aktywację szlaku MAPK/ERK przyczynia się do śmierci neuronów wywołanej przez mikroglej zubożony w TDP-43. Komórka. Śmierć Dis. 6:e1702. 10.1038/cddis.2015.69 [PMC bezpłatny artykuł] [PubMed] [CrossRef] [Google Scholar]
39. Yang S., Zhang D., Yang Z., Hu X., Qian S., Liu J. i in. (2008). Kurkumina chroni neuron dopaminergiczny przed neurotoksycznością indukowaną przez LPS w pierwotnej hodowli neuronów/gleju szczura. Neurochem. Rez. 33 2044–2053. 10.1007/s11064-008-9675-z [PubMed] [CrossRef] [Google Scholar]
40. Zhang J., Fu B., Zhang X., Zhang L., Bai X., Zhao X., et al. (2014). Bicyklol zwiększa ekspresję czynnika transkrypcyjnego Nrf2 HO-1 i chroni mózgi szczurów przed ogniskowym niedokrwieniem. Mózg Res. Byk. 100 38–43. 10.1016/j.brainresbull.2013.11.001 [PubMed] [CrossRef] [Google Scholar]
41. Zhou J., Miao H., Li X., Hu Y., Sun H., Hou Y. (2017). Kurkumina hamuje zapalenie łożyska w celu złagodzenia niekorzystnych wyników ciąży wywołanych przez LPS u myszy poprzez regulację w górę fosforylowanego Akt. stan zapalny Rez. 66 177–185. 10.1007/s00011-016-1004-4 [PubMed] [CrossRef] [Google Scholar]
Dyskusja na dodatkowe tematy: Przewlekły ból
Nagły ból jest naturalną reakcją układu nerwowego, która pomaga wykazać możliwe obrażenia. Na przykład sygnały bólowe przemieszczają się z uszkodzonego regionu przez nerwy i rdzeń kręgowy do mózgu. Ból jest zwykle mniej dotkliwy, ponieważ obrażenia się goją, jednak ból przewlekły różni się od przeciętnego rodzaju bólu. W przypadku przewlekłego bólu ciało ludzkie będzie nadal wysyłać sygnały bólu do mózgu, niezależnie od tego, czy rana się zagoiła. Przewlekły ból może trwać od kilku tygodni do nawet kilku lat. Przewlekły ból może ogromnie wpłynąć na mobilność pacjenta i może zmniejszyć elastyczność, siłę i wytrzymałość.
Neural Zoomer Plus na choroby neurologiczne
Dr Alex Jimenez wykorzystuje serię testów do oceny chorób neurologicznych. Neural ZoomerTM Plus to szereg neurologicznych autoprzeciwciał, które oferują specyficzne rozpoznawanie przeciwciał przeciw antygenowi. Vibrant Neural ZoomerTM Plus jest przeznaczony do oceny indywidualnej reaktywności na 48 antygenów neurologicznych związanych z różnymi chorobami neurologicznymi. Wibrujący zoom neuronowyTM Plus ma na celu zmniejszenie stanów neurologicznych poprzez zapewnienie pacjentom i lekarzom niezbędnych zasobów do wczesnego wykrywania ryzyka i większego nacisku na spersonalizowane pierwotne zapobieganie.
Formuły na wsparcie metylacji
XYMOGEN's Ekskluzywne profesjonalne formuły są dostępne za pośrednictwem wybranych licencjonowanych pracowników służby zdrowia. Sprzedaż internetowa i rabat na formuły XYMOGEN są surowo zabronione.
Dumnie, Dr Alexander Jimenez sprawia, że formuły XYMOGEN są dostępne tylko dla pacjentów pod naszą opieką.
Zadzwoń do naszego biura, abyśmy wyznaczyli konsultację lekarza w celu uzyskania natychmiastowego dostępu.
Jeśli jesteś pacjentem Klinika Urazów Medycznych i Chiropraktyki, możesz zapytać o XYMOGEN dzwoniąc 915-850-0900.
Dla Twojej wygody i przeglądu XYMOGEN produkty przejrzyj poniższy link. *XYMOGEN-Katalog-Do pobrania
* Wszystkie powyższe zasady XYMOGEN pozostają w mocy.
Zrzeczenie się odpowiedzialności
Profesjonalny zakres praktyki *
Informacje zawarte w niniejszym dokumencie na temat „Funkcjonalna neurologia: kurkumina na zapalenie mózgu„ nie ma na celu zastąpienia relacji jeden na jeden z wykwalifikowanym pracownikiem służby zdrowia lub licencjonowanym lekarzem i nie jest poradą medyczną. Zachęcamy do podejmowania decyzji dotyczących opieki zdrowotnej na podstawie badań i współpracy z wykwalifikowanym pracownikiem służby zdrowia.
Informacje o blogu i zakres dyskusji
Nasz zakres informacji ogranicza się do chiropraktyki, układu mięśniowo-szkieletowego, akupunktura leki fizykalne, wellness, przyczyniające się etiologiczne zaburzenia trzewno-somatyczne w prezentacjach klinicznych, powiązanej dynamice klinicznej odruchu somato-trzewnego, kompleksach podwichnięć, wrażliwych kwestiach zdrowotnych i/lub artykułach, tematach i dyskusjach z zakresu medycyny funkcjonalnej.
Zapewniamy i prezentujemy współpraca kliniczna ze specjalistami z różnych dziedzin. Każdy specjalista podlega zakresowi swojej praktyki zawodowej i jurysdykcji licencyjnej. Stosujemy protokoły funkcjonalnego zdrowia i dobrego samopoczucia, aby leczyć i wspierać opiekę nad urazami lub zaburzeniami układu mięśniowo-szkieletowego.
Nasze filmy, posty, tematy, tematy i spostrzeżenia obejmują kwestie kliniczne, problemy i tematy, które bezpośrednio lub pośrednio odnoszą się do naszego zakresu praktyki klinicznej i wspierają ją.*
Nasze biuro rozsądnie próbowało podać cytaty potwierdzające i zidentyfikowało odpowiednie badania naukowe potwierdzające nasze posty. Na żądanie udostępniamy kopie badań wspierających, które są dostępne dla organów regulacyjnych i opinii publicznej.
Rozumiemy, że zajmujemy się sprawami, które wymagają dodatkowego wyjaśnienia, w jaki sposób może to pomóc w konkretnym planie opieki lub protokole leczenia; w związku z tym, aby dokładniej omówić powyższy temat, prosimy o kontakt Dr Alex Jimenez, DC, lub skontaktować się z nami pod adresem 915-850-0900.
Jesteśmy tutaj, aby pomóc Tobie i Twojej rodzinie.
Błogosławieństwa
Dr Alex Jimenez OGŁOSZENIE, MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
e-mail: coach@elpasofunctionmedicine.com
Licencjonowany jako lekarz chiropraktyki (DC) w Texas & Nowy Meksyk*
Licencja Texas DC nr TX5807, Licencja DC w Nowym Meksyku nr NM-DC2182
Licencjonowana pielęgniarka dyplomowana (RN*) w Floryda
Licencja Floryda Licencja RN nr RN9617241 (nr kontrolny 3558029)
Stan kompaktowy: Licencja wielostanowa: Uprawniony do wykonywania zawodu Stany 40*
Obecnie immatrykulowany: ICHS: MSN* FNP (Program Praktyk Pielęgniarki Rodzinnej)
Dr Alex Jimenez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Moja cyfrowa wizytówka






 Znowu witamy¸
Znowu witamy¸
